細(xì)胞因子TNF-α(TNF-α)在亞nM濃度下容易形成同源三聚體以促進(jìn)炎癥。為了治療TNF-α水平上調(diào)的炎性疾病,目前使用許多治療性抗體作為清除劑以降低患者中的活性TNF-α濃度。盡管它們的臨床成功,不同抗體形式在穩(wěn)定三聚體狀態(tài)方面的作用模式尚未完全了解。在這里,我們使用具有動態(tài)納米桿的生物傳感器來分析TNF-α的單體和三聚體狀態(tài)以及治療性生物制劑的結(jié)合動力學(xué)。1.7 × 10?3 s?1可以直接使用heliX系統(tǒng)測量,并在pM范圍內(nèi)分析抗體結(jié)合親和力。阿達(dá)木單抗、英夫利昔單抗、依那西普、賽妥珠單抗、戈利木單抗的二價和單價結(jié)合形式的三聚體穩(wěn)定效應(yīng)被量化。觀察到三聚體穩(wěn)定性的明顯差異,這可能為深入了解TNF-α清除劑的作用模式提供了更深入的見解
TNFTNF-α是一個細(xì)胞因子,在介導(dǎo)炎癥過程中起著關(guān)鍵作用.TNF-α的單體亞單位在溶液中以亞納摩爾濃度形成穩(wěn)定的非共價同源三聚體。內(nèi)源性TNF受體(TNFR)1和2通過識別TNF-α三聚體進(jìn)行信號傳遞,TNFR 1和2在與TNF-α形成復(fù)合物之前形成三聚體。已知三聚體TNF-α在低濃度下隨時間單體化。其導(dǎo)致生物活性的喪失。在患有多種不同自身免疫性疾病的患者中發(fā)現(xiàn)TNF-α表達(dá)水平升高.抗TNF-α的清除性抗體和抗原結(jié)合片段(Fab)已被證明能成功抑制TNF-α的表達(dá)。包括類風(fēng)濕性關(guān)節(jié)炎、銀屑病和克羅恩病在內(nèi)的炎性自身免疫疾病中介導(dǎo)的炎癥。
盡管治療性抗體形式之間存在顯著的結(jié)構(gòu)差異:英夫利西單抗、阿達(dá)木單抗、塞妥珠單抗和依那西普,研究表明,所有四種生物分子均通過與人細(xì)胞上的膜結(jié)合TNF-α結(jié)合參與反向信號轉(zhuǎn)導(dǎo),盡管依那西普和塞妥珠單抗不能交聯(lián)任何類型的TNF-α三聚體.阿達(dá)木單抗Fab和英夫利西單抗Fab與單個TNF-α三聚體的多個結(jié)合事件的結(jié)構(gòu)差異表明,TNF三聚體與阿達(dá)木單抗Fab復(fù)合物的穩(wěn)定性更強(qiáng),其結(jié)合在兩個單體亞單位之間的界面上,而每個英夫利西單抗Fab與TNF-α三聚體中的單個單體亞單位結(jié)合。交聯(lián)似乎與誘導(dǎo)細(xì)胞凋亡無關(guān),因?yàn)轶w外試驗(yàn)顯示,對于英夫利西單抗,F(xiàn)ab和完整IgG之間沒有顯著差異。利用分子排阻色譜法(SEC)進(jìn)行的試驗(yàn)可以顯示,二價TNF-α結(jié)合劑(如阿達(dá)木單抗、英夫利西單抗和戈利木單抗)能夠形成由三個IgG分子連接的三種可溶性TNF-α三聚體的高度穩(wěn)定復(fù)合物。關(guān)于TNF-α清除劑在TNF-α寡聚體狀態(tài)下的行為,我們知之甚少。
在這項(xiàng)研究中,研究人員對TNF-a單聚化和重三聚化的實(shí)時動力學(xué)進(jìn)行研究。之前的研究重點(diǎn)關(guān)注平衡狀態(tài)下的單體交換率,采用F?rster共振能量轉(zhuǎn)移(FRET)以及分析性尺寸排阻層析分析。與這些研究相反,我們使用新型電可切換生物表面技術(shù)(ESB)通過實(shí)時連續(xù)測量來確定通用單體化率。由于與其清除劑復(fù)合時,TNF-a的單聚化反映了自由TNF-a的增加,因此我們研究了TNF-a-三聚體-TNF-cleaner復(fù)合物與阿達(dá)木單抗、英夫利西單抗、戈利木單抗、塞托珠單抗和依那西普以及源自阿達(dá)木單抗、英夫利西單抗和戈利木單抗的Fab片段的穩(wěn)定性。我們發(fā)現(xiàn)TNF-a可以在活性三聚體和非活性單體之間快速切換,這揭示了一種新的、快速作用的方式來調(diào)節(jié)其生物活性。有趣的是,治療性抗體形式及其Fabs的三聚體穩(wěn)定性存在很大差異。有些不會(完全)抑制結(jié)合的TNF-a的單體化,從而導(dǎo)致TNF-a單體的釋放。這些TNF-a的單體亞基尚未顯示形成臨床相關(guān)量的三聚體TNF-a。然而,在體外實(shí)驗(yàn)中,已經(jīng)證明了濃度依賴性的重三聚化。
為了評估TNF-α的寡聚狀態(tài),將蛋白質(zhì)以500 nM的濃度固定到傳感器表面,該濃度顯著高于亞納摩爾三聚KD以避免單體化。在誘導(dǎo)單體化之前,在四個重復(fù)中測定固定化TNF-α的大小,得到初始狀態(tài)的流體動力學(xué)直徑為5.6± 0.1 nm(圖1B,t0)。該值與基于TNF-α三聚體PDB結(jié)構(gòu)的流體動力學(xué)直徑的計(jì)算預(yù)測非常一致,其產(chǎn)生的DH值為5.76 nm(3ALQ)至6.10 nm(1 TNF)。接著,通過以1 ml/min的流速注射運(yùn)行緩沖液2000 s,引發(fā)固定化TNF-α的單體化,由于TNF-α亞基的解離,導(dǎo)致轉(zhuǎn)換速度逐漸增加(流體動力學(xué)摩擦降低)(圖1C)。與之前報道的三聚體TNF-a之間在小時范圍內(nèi)緩慢的單體交換相反,發(fā)現(xiàn)純單體化在30分鐘內(nèi)發(fā)生,產(chǎn)生單體化率k=1.66±0.25 10- 3s-1。緩沖液流動后,通過測定單體TNF-a的流體動力學(xué)直徑來評價單體化效率,所得DH為3.5至4.0納米(t1,圖1B)。再次,發(fā)現(xiàn)該值與基于單體TNF-a的DBC結(jié)構(gòu)的計(jì)算預(yù)測(4.39納米,4G3Y; 4.44納米,3WD5)非常一致。這表明在實(shí)驗(yàn)過程中,實(shí)現(xiàn)了完全的單體化。
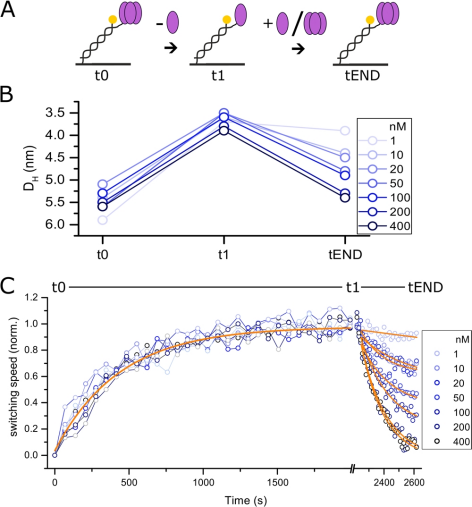
圖1. TNF-a的單體化和再三聚動力學(xué)。通過與表面束縛的互補(bǔ)DNA鏈雜交來固定化TNF-a-DNA結(jié)合物,通過緩沖液流進(jìn)行單體化,然后重新三聚化(A)。通過測量流體動力學(xué)直徑,確定固定化的TNF-a(t0)、單體化復(fù)合物(t1)和與納摩爾濃度的自由TNF-a作用的復(fù)合物(tEnd)的尺寸(B)。在初始狀態(tài)下,固定化的TNF-a的尺寸確定產(chǎn)生5.6±0.1nm的流體動力學(xué)直徑,而在緩沖液流動2000 s后,確定較小的尺寸,對應(yīng)于3.9±0.1nm的單體TNF-a。注射更高納摩爾濃度的自由TNF-a可誘導(dǎo)有效的三聚體形成,使轉(zhuǎn)變成為一個可逆的過程。單體化動力學(xué)的單指數(shù)模擬得到的單體化速率為1.66±0.25 E-3 s-1(C,橙色實(shí)心線,t0至t1)。高納摩爾濃度的自由TNF-a導(dǎo)致在不到600 s內(nèi)快速重新三聚化(C,t1至tEnd)。
將固定化的單體TNF-a置于不同濃度的自由TNF-a中,以解析三聚動力學(xué)(圖2)。1C,tl-tEnd)。正如之前報道的那樣,TNF-a的單體化和三聚化是一個完全可逆的過程。在這里,發(fā)現(xiàn)三聚體形成的開始發(fā)生在約10 ns的自由TNF-a(175 ng/ml,圖1B、C)下。這些發(fā)現(xiàn)與使用基于FRET的分析的三聚體穩(wěn)定性評估一致,顯示在平衡條件下,濃度高達(dá)300 ng/ ml時三聚體狀態(tài)略有損失。當(dāng)濃度高于200 ns(3.5 μg/ml)時,可以在幾分鐘內(nèi)重新獲得完整的三聚體(圖1B、C、t1-tEnd)。這些實(shí)驗(yàn)中確定的TNF-a單聚和三聚的時間表比之前報道的文獻(xiàn)短得多。這可能反映了對促炎癥觸發(fā)物通常快速進(jìn)行的反應(yīng)。
在分析了TNF-a單體化的動態(tài)性質(zhì)后,我們研究了TNF-a的低聚狀態(tài)對最常見的針對TNF-a的治療性抗體(即阿達(dá)木單抗)動力學(xué)的影響。為了降低這種相互作用的復(fù)雜性,我們通過用木瓜蛋白酶進(jìn)行有限的蛋白酶切割來制備阿達(dá)木單抗的Fab片段,以創(chuàng)建一種簡化的環(huán)境,其中至少一種相互作用伴侶(此處為阿達(dá)木單抗Fab)是單價的。為了簡化分析,文獻(xiàn)中通常通過固定抗體來避免親合力(和交叉)效應(yīng)。然而,對于這個生物系統(tǒng)來說,多價結(jié)合不容忽視,但解決它至關(guān)重要(見示意圖、圖。2和3)。

圖2. TNF-a-阿達(dá)木單抗Fab相互作用。以反向(固定化的TNF-a,A)和正向試驗(yàn)方向(固定化的Fab片段,B)記錄了TNF-a與阿達(dá)木單抗Fab的相互作用。注射在運(yùn)行緩沖液(1、2、4、8 ns)中稀釋的阿達(dá)木單抗Fab(A)或TNF-a(B)溶液260秒(結(jié)合),然后注射運(yùn)行緩沖液18,000秒(分離)。純淺灰色至黑線(1至8 Mb)代表標(biāo)準(zhǔn)化數(shù)據(jù)。橙色實(shí)線代表全球貼合數(shù)據(jù)。表1列出了動態(tài)率、親和力和幅度。
首先,我們研究了單價阿達(dá)木單抗Fab在兩個方向上與三聚體TNF-a結(jié)合的更簡單情況。在相反的試驗(yàn)方向中,阿達(dá)木單抗Fab與固定化三聚體TNF-a的結(jié)合動力學(xué)(圖2A)可以通過單指數(shù)函數(shù)描述。與固定配體的每個結(jié)合事件都是獨(dú)立檢測的,這對應(yīng)于1:1的相互作用。Fabs從部分飽和表面(注射1和2 nM Fab)的分解動力學(xué)是雙相的,具有快速和緩慢的速度,分別為kFast=1.42±0.39 10- 3s-1和kSLOW =8.52±0.28 10- 5s-1(圖2A和S3)。快速的分離率類似于之前確定的TNF-a單聚化率,并且很可能源于未被結(jié)合的Fab穩(wěn)定的TNF-a三聚體的衰變。緩慢的速度可以歸因于Fab與固定化的TNF-a三聚體的分離,這可以通過與圖*中相反的檢測方向進(jìn)行比較來看出。在這里,發(fā)現(xiàn)了與固定化阿達(dá)木單抗Fab的分離率相同的速率。正如預(yù)期的那樣,沒有觀察到快速單體化。相反,可觀察到的動力學(xué)表明第三個甚至更慢的分解過程,這是可感知的,因?yàn)樾盘栐?8,000秒的運(yùn)行時間內(nèi)沒有接近基線。這可以用親合效應(yīng)來解釋,即兩個或三個固定的阿達(dá)木單抗Fab通過一個緊密結(jié)合的三聚體TNF-a相互連接。已知固定阿達(dá)木單抗Fab的多價結(jié)合形成高度穩(wěn)定的復(fù)合物。
然后,我們研究了完整阿達(dá)木單抗Iggs的親和力對與TNF-a相互作用的影響。之前的研究描述了三個阿達(dá)木單抗分子與三個TNF-a三聚體結(jié)合形成的高度穩(wěn)定的復(fù)合物。然而,這些復(fù)合物對相互作用參數(shù)的影響以及在其中一個分子被固定的情況下是否形成這些復(fù)合物是這里研究的主題。在兩種試驗(yàn)方向中,由于TNF-a和阿達(dá)木單抗IgGs固有的多價特性,可能發(fā)生多重結(jié)合(圖3A、B)。阿達(dá)木單抗全抗體和TNF-a的相互作用測量結(jié)果顯示,兩個方向上的速率常數(shù)相當(dāng)(表1)。此外,與上圖*中的親力相容性試驗(yàn)設(shè)置類似,阿達(dá)木單抗的兩個方向均表現(xiàn)出降低的分離幅度,表明形成了相互關(guān)聯(lián)的復(fù)合物。
表1列出了確定的TNF-a和阿達(dá)木單抗Fab/完整阿達(dá)木單抗抗體之間相互作用的動力學(xué)速率和親和力。溶液中固定化阿達(dá)木單抗IgG和TNF-a的解離速率常數(shù)與已發(fā)表的數(shù)據(jù)完全一致。作為一個重要的結(jié)果,我們觀察到兩種檢測方向的一致親和力和相似的速率,首次表明方向不會顯著影響結(jié)合模式及其親和力。
完整阿達(dá)木單抗抗體抗體與其Fab結(jié)合固定化TNF-a的結(jié)合速率常數(shù)的差異可以通過在Fab結(jié)合的情況下,IgG的第二次結(jié)合事件不存在“錨定效應(yīng)”來解釋。自然,由于結(jié)合第一個Fab-臂(第二個Fab-臂的“強(qiáng)制接近”)后第二個Fab-臂的局部濃度大幅增加,因此IgGs的第二個結(jié)合事件以急劇增加的速度發(fā)生。
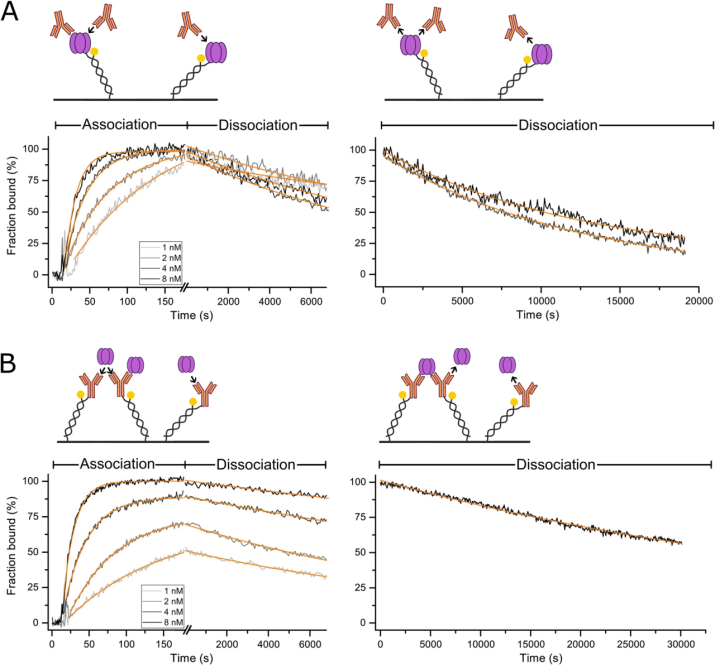
圖3. TNF-a-阿達(dá)木單抗相互作用。以反向(固定化的TNF-a,A)和正向試驗(yàn)方向(固定化的阿達(dá)木單抗IgG,B)記錄了TNF-a與阿達(dá)木單抗的相互作用。記錄的關(guān)聯(lián)時間為160秒,分離時間為7200秒。此外,對于最高分析物濃度,記錄了18,000 s(A)和30,000 s(B)的更長的分解階段。分析物溶液以1、2、4、8 ns(淺灰色至黑線)的濃度進(jìn)樣。橙色線代表適合數(shù)據(jù)。
表1列出了動態(tài)率和幅度。
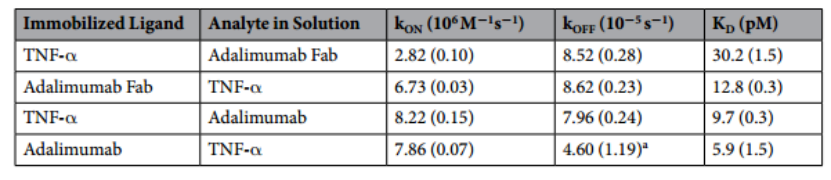
表1.動力學(xué)速率常數(shù)、解離常數(shù)。誤差是單獨(dú)匹配kOFF的平均值的標(biāo)準(zhǔn)誤差
作為之前描述的結(jié)合動力學(xué)測量的補(bǔ)充方法,我們通過溶液滴度進(jìn)行了親和力測量,這排除了由于固定化過程而可能出現(xiàn)的偽影。將TNF-a和抗體以不同比例混合在溶液中并允許結(jié)合。平衡后,生物傳感器以濃度測量模式測量未結(jié)合的TNF-a的剩余分?jǐn)?shù)。在這里,我們使用固定化阿達(dá)木單抗來檢測在具有恒定濃度的TNF-a和增加濃度的阿達(dá)木單抗預(yù)孵育的溶液中剩余的具有結(jié)合能力的TNF-a(-復(fù)合物)(圖4A)。進(jìn)行此類實(shí)驗(yàn)的困難在于兩種結(jié)合劑的多價性(TNF-a三聚體= 3,阿達(dá)木單抗= 2),這導(dǎo)致形成更高級的復(fù)合物,正如之前所描述的那樣(形成由三個阿達(dá)木單抗IgGs互連的三個TNF-a三聚體)。由多個TNF-a和多個阿達(dá)木單抗分子組成的幾種不同復(fù)合物可以被表面束縛的阿達(dá)木單抗結(jié)合,這就是為什么圖4A中采用的簡單1:1匹配模型低估了劑量反應(yīng)的陡峭性,只能被認(rèn)為是一種近似。此外,TNF-a的濃度應(yīng)該在生物學(xué)相關(guān)范圍內(nèi)(必須存在三聚體),但要低到足以仍然到達(dá)KD敏感區(qū)域。對于這里的實(shí)驗(yàn),選擇c(TNF-a)為100 pM和500 pM。溶液親和力測量證實(shí)了動力學(xué)實(shí)驗(yàn)中確定的解離常數(shù),KD(c(TNF-a)= 100 pM)= 53.6±29.5 pM; KD(c(TNF-a)= 500 pM)< 30.0 pM)(圖4 B)。
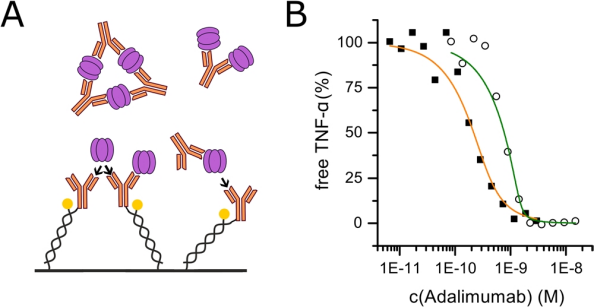
圖4.溶液平衡滴度親和力測量。可溶性TNF-a與可溶性阿達(dá)木單抗的結(jié)合(A)。將恒定濃度的TNF-a(100 pM,實(shí)心正方形和500 pM,空心圓)與不同濃度的阿達(dá)木單抗(7 pM至15 ns)混合并孵育7.5小時。將混合物注射到表面固定化阿達(dá)木單抗中,以確定自由TNF-a的殘留濃度。將線性結(jié)合曲線的斜坡標(biāo)準(zhǔn)化并相對于可溶性阿達(dá)木單抗?jié)舛壤L制繪圖。從S形轉(zhuǎn)變,確定溶液中Adalimumab-TNF-a結(jié)合的電離常數(shù)(KD(c(TNF-a)= 100 pM)= 53.6±29.5 pM; KD(c(TNF-a)= 500 pM)<30.0 pM)(B)。
在表征多價性對TNF-α-阿達(dá)木單抗/阿達(dá)木單抗Fab相互作用中相互作用參數(shù)的影響后,我們研究了TNF-α與5種不同抗TNF-α抗體及其Fab片段復(fù)合物的單體化。為此,將TNF-α固定在傳感器表面上,并用5 nM相應(yīng)的TNF-α清除劑飽和。然后,將表面連續(xù)暴露于TNF-α清除劑(5 nM)以確保清除劑不能有效地從表面解離。這樣,轉(zhuǎn)換速度信號的增加表明清除劑結(jié)合的TNF-α的衰減,但不是清除劑解離。開關(guān)速度監(jiān)測70分鐘。觀察到所有的TNF-a狂熱結(jié)合物(阿達(dá)木單抗、英夫利西單抗、戈利木單抗)的單體化完全抑制(轉(zhuǎn)換速度沒有增加),這些結(jié)合物可以形成相互關(guān)聯(lián)的多重結(jié)合復(fù)合物(圖5,純藍(lán)色、品紅色和綠色符號)。阿達(dá)木單抗和英夫利西單抗的這些發(fā)現(xiàn)與文獻(xiàn)一致。然而,在FRET試驗(yàn)中,與戈利木單抗復(fù)合物中,TNF-a單體化速度更快被發(fā)現(xiàn)。我們僅在源自戈利木單抗的Fab片段中觀察到這種行為,其對單體化的抑制最弱(圖5,開放綠色符號)。與自由單體化率(圖5,灰色符號)相比,與戈利木單抗Fab復(fù)合的率僅降低了三倍。相比之下,來自阿達(dá)木單抗和英夫利西單抗的Fab片段對單體化表現(xiàn)出更強(qiáng)的抑制作用(圖5,空心藍(lán)色和品紅色符號)。受控消化抑制了相互連接,但英夫利西單抗Fab和阿達(dá)木單抗Fab的單聚率仍然剛剛提高到可檢測水平(kMONO=4.0E-5 s-1)(圖5,空心藍(lán)色和品紅色符號)。Van Schie還描述了在Certolumab存在下的中等快速單體化。Scallon等人發(fā)現(xiàn),在Etanercept的存在下,放射性標(biāo)記的TNF-a可以快速替代。在這里,兩種不代表完整抗體的治療形式,即塞爾托珠單抗和依那西普,都顯示出中等快速的單體化(圖5,分別是空心黑色和實(shí)心橙色符號)。
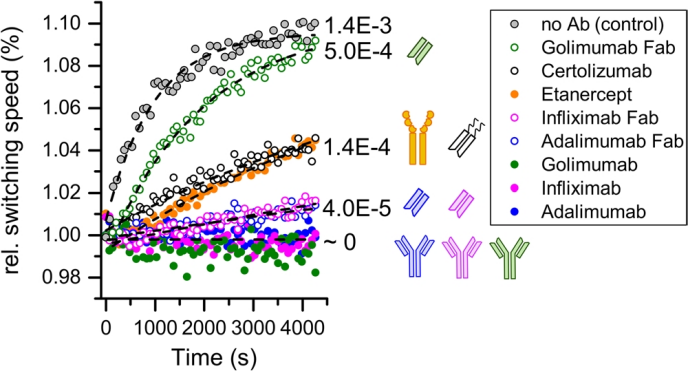
圖5.通過治療性抗體形式穩(wěn)定TNF-a三聚體。將TNF-a固定在傳感器表面上,并用5 InM相應(yīng)的TNF-a清除劑飽和;緩沖液注射作為無抗體對照。在恒定背景濃度為5 nM的TNF-cleaner下,以1 ml/min的流速記錄了TNF-a-TNF-a-TNF-a-cleaner復(fù)合物中的TNF-a的單體化4200 s。一式三份進(jìn)行測量并取平均值。單體化率(s-1)取自單指數(shù)曲線(黑色虛線)。
在這項(xiàng)研究中,我們研究了TNF-α寡聚體狀態(tài)轉(zhuǎn)換的動力學(xué)。基于以前的研究,報道了TNF-α的單體化是在數(shù)小時的時間尺度上發(fā)生的過程。雖然純單體化率尚未確定,但只研究了TNF-α三聚體之間單體亞單位交換的監(jiān)測。在這里,我們提供了在幾分鐘的時間尺度上,TNF-α的生物活性形式和非活性形式之間相對快速轉(zhuǎn)變的數(shù)據(jù)。
這種單體化的實(shí)時評估可能有助于更深入地了解通過調(diào)節(jié)TNF-α的生物活性對炎癥的整體調(diào)節(jié)。TNF-α寡聚體狀態(tài)的濃度依賴性調(diào)節(jié)的高度動態(tài)性質(zhì)允許在確定的區(qū)室中產(chǎn)生強(qiáng)烈的免疫反應(yīng),而不會遇到全身性炎癥的風(fēng)險。TNF-α三聚體通過在較低血清水平下快速分解表現(xiàn)出的生物活性的快速喪失而具有一種內(nèi)在的保護(hù)性開關(guān)。迄今為止,準(zhǔn)確測定生物樣品中的細(xì)胞因子濃度仍然是一項(xiàng)具有挑戰(zhàn)性的任務(wù)。因此,此處顯示的體外再三聚化實(shí)驗(yàn)的絕對TNF-α濃度的比較是不可靠的。
此外,TNF-α三聚體的快速形成和衰減使得復(fù)雜溶液中的精確定量更加困難。在平衡條件下,TNF-α-阿達(dá)木單抗和TNF-α-阿達(dá)木單抗Fab復(fù)合物中單體化的一般抑制已經(jīng)用HP-SEC和FRET分析進(jìn)行了表征。然而,F(xiàn)RET測量不能區(qū)分單體化的抑制是高級寡聚復(fù)合物(例如三個TNF-α三聚體和三個阿達(dá)木單抗分子的熱最穩(wěn)定的等摩爾復(fù)合物)形成的產(chǎn)物,還是由三聚體內(nèi)TNF-α單體亞單位界面中單個阿達(dá)木單抗(Fab)分子結(jié)合引起的。從動力學(xué)實(shí)驗(yàn)(圖2和圖3)可以明顯看出,無論何時TNF-α被各自的拮抗劑飽和,在兩種檢測方向上,全阿達(dá)木單抗IgG和阿達(dá)木單抗Fab都發(fā)生了單體化的抑制。
然而,我們在TNF-α-阿達(dá)木單抗/阿達(dá)木單抗Fab相互作用中觀察到正向和反向測定方向之間的兩個實(shí)質(zhì)性差異。阿達(dá)木單抗Fab與固定化TNF-α的結(jié)合速率明顯低于所有其他相互作用。完整阿達(dá)木單抗IgG與其Fab結(jié)合固定化TNF-α的結(jié)合速率常數(shù)的差異可以用Fab結(jié)合時IgG第二結(jié)合事件的“錨定效應(yīng)”的缺失來描述。自然地,IgG的第二結(jié)合事件以急劇增加的速率發(fā)生,這是由于在結(jié)合第一Fab時第二Fab的局部濃度強(qiáng)烈增加(“第二Fab的被迫接近”)。此外,相對解離幅度存在差異:只有排除固定配體分子的“橋接”(圖2A),才能實(shí)現(xiàn)完全解離。據(jù)我們所知,阿達(dá)木單抗全I(xiàn)gG和阿達(dá)木單抗Fab與TNF-α相互作用的動力學(xué)分析和比較是皮摩爾結(jié)合物的首次相互作用分析,其速率常數(shù)一致,與檢測方向無關(guān)。除此之外,對于停留時間> 10,000 s的抗體或fab,以前沒有顯示完全解離。只有協(xié)同使用二維配體分布、固定抗原的低表面密度和非常高的流速,才能抑制分析物不可避免的再結(jié)合,從而損害解離幅度和速率。然而,即使通過優(yōu)化實(shí)驗(yàn)設(shè)計(jì),兩種多價結(jié)合物如TNF-α及其清除劑抗體的表征和定量分析仍然是一項(xiàng)具有挑戰(zhàn)性的任務(wù)。
在以單價阿達(dá)木單抗Fab作為可溶性分析物分子的分析中,可以排除包含多個TNF-α三聚體的復(fù)合物的形成。因此,我們得出結(jié)論,單體化的抑制不僅僅是高階復(fù)合物形成的產(chǎn)物。我們的數(shù)據(jù)表明,TNF-α清除劑與TNF-α三聚體中單個單元之間的界面凹槽的結(jié)合足以抑制單體化。
基于阿達(dá)木單抗Fab和英夫利昔單抗Fab與TNF-α復(fù)合物的晶體結(jié)構(gòu),預(yù)計(jì)在單體化抑制方面有很大差異。阿達(dá)木單抗Fab明顯結(jié)合在亞單位的界面上,而英夫利昔單抗Fab僅結(jié)合單個亞單位。本研究中三聚體穩(wěn)定的功能分析不能檢測阿達(dá)木單抗Fab或英夫利昔單抗Fab之間的差異,也不能檢測親本IgG之間的差異(圖5)。
Ono等人的數(shù)據(jù)顯示,與TNF-α三聚體的單體亞單位的界面結(jié)合是Golimumab、TNFR2和Certolizumab的共同特性。在這里,我們觀察到在Golimumab Fab、Certolizumab和依那西普的復(fù)合物中對單體化的抑制作用較弱。TNF-α拮抗劑對TNF-α三聚體的不同穩(wěn)定作用可能在優(yōu)化這些清除劑的治療應(yīng)用中發(fā)揮作用。
本研究中的實(shí)驗(yàn)均通過 heliX + 分子互作分析系統(tǒng)完成




