由新型冠狀病毒(SARS-CoV-2)感染引起的急性呼吸系統(tǒng)綜合癥,對人類的生命健康產(chǎn)生了極大威脅。病毒顆粒的刺突蛋白(Spike)與人類的血管緊張素轉(zhuǎn)化酶2(hACE2)分子受體相互作用,是病毒感染入侵人體的主要機(jī)制。為了深入研究其相互作用及動力學(xué)機(jī)制,本文利用傳統(tǒng)酶聯(lián)免疫吸附檢測技術(shù)(ELISA)及新型熒光距離感應(yīng)技術(shù)(SwitchSENSE),從以下四方面對分子間的相互作用動力學(xué)進(jìn)行了詳盡的評估:
-
全長的病毒刺突蛋白,僅含有蛋白的RBD結(jié)構(gòu)域以及僅含有S1亞基的片段與hACE2受體蛋白肽的結(jié)合差異;
-
兩種分子之間的單價(jià)互作與兩分子的三價(jià)形式互作之間的動力學(xué)差異;
-
刺突蛋白的氨基酸序列突變對互作動力學(xué)的影響;
-
hACE2受體肽和失活的冠狀病毒顆粒及假病毒顆粒之間的互作動力學(xué);
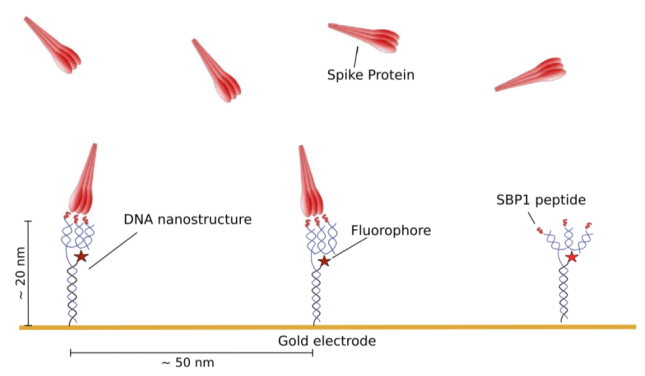
SwitchSENSE技術(shù)的實(shí)驗(yàn)設(shè)計(jì)模式圖總覽
熒光距離接近感應(yīng)SwitchSENSE技術(shù)是由德國Dynamic Biosensor生物技術(shù)公司開發(fā)的一種基于微流控芯片的分子互作技術(shù)。該技術(shù)以耦合在生物芯片上的DNA納米桿為載體,納米桿可同時(shí)攜帶熒光基團(tuán)及分子互作配體。芯片在處于合適的電場中時(shí),DNA納米桿可保持直立靜止的狀態(tài);當(dāng)含有底物的緩沖液在微流控作用下流經(jīng)芯片表面時(shí),配體與底物分子發(fā)生相互作用,該相互作用改變了熒光基團(tuán)所處的化學(xué)環(huán)境,導(dǎo)致熒光信號發(fā)生變化。該變化的熒光信號通過儀器對發(fā)出的光子進(jìn)行捕捉并計(jì)數(shù),進(jìn)而對分子間相互作用動力學(xué)及親和性進(jìn)行實(shí)時(shí)的檢測。
相較于傳統(tǒng)的ELISA半定量技術(shù),該技術(shù)可對光子數(shù)進(jìn)行絕對測量;同時(shí),由于DNA分子的柔韌性及堿基互補(bǔ)配對原理,使得在芯片表面固定多價(jià)分子(參見模式圖)成為可能。這也是本文應(yīng)用SwitchSENSE技術(shù)進(jìn)行該研究的優(yōu)勢之一。
在病毒入侵和感染的過程中,關(guān)于病毒表面刺突蛋白與呼吸道組織細(xì)胞膜受體蛋白的相互作用研究十分重要。能夠與刺突蛋白進(jìn)行互作的蛋白多肽,在相關(guān)研究或診斷治療中,都是十分有價(jià)值的工具。尤其是模擬刺突蛋白與細(xì)胞表面受體結(jié)合序列的多肽,能夠抑制病毒顆粒對宿主細(xì)胞的黏附和融合。本文用于進(jìn)行相關(guān)研究的SBP1多肽,來自于hACE2蛋白氨基端的a螺旋序列,由23個(gè)氨基酸構(gòu)成。已經(jīng)報(bào)道,SBP1與SARS-CoV-2的受體結(jié)合域(RBD)存在uM級的親和性。本文在已有研究的基礎(chǔ)上,進(jìn)一步測定了SBP1與刺突蛋白不同亞單位,以及與含有不同突變的刺突蛋白之間的互作效應(yīng)。
本研究中使用了以DNA納米桿為結(jié)構(gòu)基礎(chǔ)的SwitcSENSE技術(shù),該技術(shù)的優(yōu)勢在于,它可以在芯片表面偶聯(lián)三價(jià)配體(此處指SBP1),與三聚刺突蛋白的表位相對應(yīng)。它非常靈活的改變芯片表面的配體偶聯(lián),使得單價(jià)偶聯(lián)和多價(jià)偶聯(lián)成為可能,而不同價(jià)位與刺突蛋白不同表位的協(xié)同結(jié)合作用,也是實(shí)際應(yīng)用中需要明確的關(guān)鍵信息。因此本文采用的策略是使用四條DNA序列,通過互相堿基互補(bǔ)配對雜交,形成能夠結(jié)合三個(gè)多肽序列的DNA納米骨架(參見模式圖)。本文同時(shí)運(yùn)用該結(jié)構(gòu)與單價(jià)偶合肽的互作進(jìn)行了動力學(xué)的比較。
在互作結(jié)合的技術(shù)選擇上,本文同時(shí)選擇了傳統(tǒng)的ELISA檢測技術(shù),同樣使用以DNA為基礎(chǔ)的肽-DNA偶聯(lián)形式,目的在于希望能夠證明這種以DNA-肽結(jié)構(gòu)的單價(jià)結(jié)合形式可以在不同的技術(shù)背景中進(jìn)行運(yùn)用,比如表面等離子共振技術(shù)(SPR),流式細(xì)胞術(shù)等。
通過四條堿基互補(bǔ)配對的DNA鏈,將SBP1-DNA納米結(jié)構(gòu)進(jìn)行整合,并通過聚丙烯酰胺凝膠電泳(PAGE)對蛋白和核酸的偶聯(lián)情況及結(jié)構(gòu)的折疊情況進(jìn)行鑒定。首先,本文將四條攜帶有配體SBP1的DNA臂固定在芯片上,然后觀測SARS-CoV-2刺突蛋白與SBP1的結(jié)合動力學(xué)。
本實(shí)驗(yàn)中分別檢測了SARS-CoV-2刺突蛋白的兩個(gè)亞基和全長蛋白與SBP1的結(jié)合。刺突蛋白包含S1和S2兩個(gè)亞基,其中S1亞基包含RBD區(qū)域,該區(qū)域經(jīng)證實(shí)為與SBP1的互作區(qū)域。本實(shí)驗(yàn)選擇S1亞基,RBD區(qū)域和全長蛋白分別進(jìn)行檢測。結(jié)果如下圖所示:
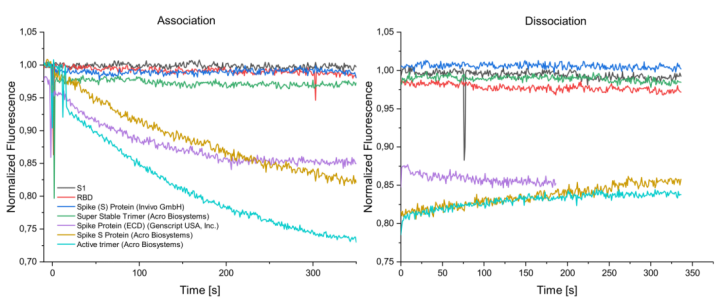
結(jié)果表明,S1亞基與RBD結(jié)構(gòu)域均未能和SBP1進(jìn)行結(jié)合,而來自不同公司的全長蛋白,SARS-CoV-2刺突蛋白(ECD),SARS-CoV-2 S蛋白和SARS-CoV-2S, active trimer與SBP1具有明顯的結(jié)合動力學(xué)表征。而兩個(gè)攜帶突變氨基酸的全長蛋白SARSCoV-2 S, Super Stable Trimer和Spike(S) protein未表現(xiàn)出結(jié)合能力。這兩種突變蛋白攜帶多個(gè)突變,包括位于Furin蛋白酶切位點(diǎn)區(qū)域的R683A,R685A突變以及K986P和K987P位點(diǎn)突變。已有報(bào)道Furin蛋白酶切位點(diǎn)對于刺突蛋白與配體的結(jié)合活性非常重要,而986和987氨基酸位點(diǎn)被證明可以阻止刺突蛋白從融合前狀態(tài)到融合后狀態(tài)構(gòu)象的變化,因此對于生物體來說是非常有利的突變。
本實(shí)驗(yàn)通過SwithSENSE和ELISA技術(shù)分別比較了全長刺突蛋白SARS-CoV-2 S protein,SARS-CoV-2 S protein, active trimer和攜帶三肽或僅攜帶一肽的DNA納米結(jié)構(gòu)的結(jié)合。結(jié)果如下圖所示:
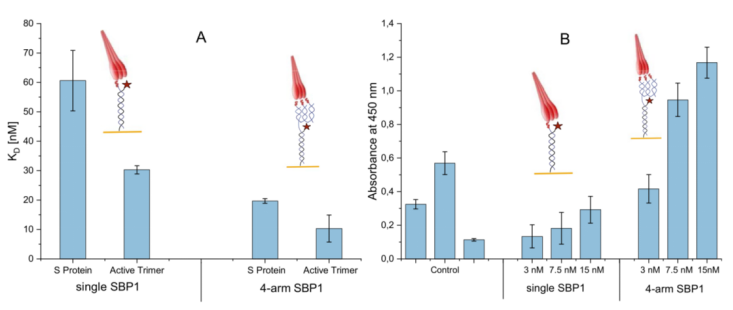
A和B分別為SwitchSENSE技術(shù)以及ELISA技術(shù)檢測結(jié)果。結(jié)果顯示,分子間的單價(jià)互作和三價(jià)互作在兩種技術(shù)中顯示出一致性,兩種全長蛋白在分子三價(jià)互作中,其動力學(xué)親和性均較單價(jià)互作強(qiáng)。具體檢測數(shù)值請見下表:
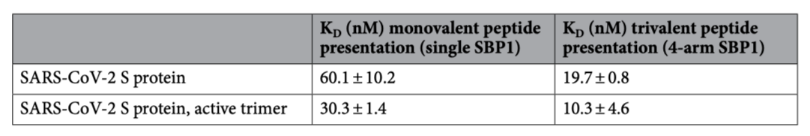
為了證明DNA-SBP1納米結(jié)構(gòu)不僅可以與溶液中的刺突蛋白進(jìn)行互作,也能夠與病毒顆粒表面的蛋白進(jìn)行結(jié)合,本實(shí)驗(yàn)使用了化學(xué)刺激失活后的病毒顆粒與攜帶三肽的DNA-SBP1納米結(jié)構(gòu)進(jìn)行動力學(xué)表征檢測。將DNA-SBP1納米結(jié)構(gòu)進(jìn)行固定,病毒顆粒溶液以不同的濃度進(jìn)行微流控上樣。由于病毒顆粒平均直徑約為90nm,而兩個(gè)DNA納米結(jié)構(gòu)之間的距離約為50nm。因此一個(gè)病毒顆粒理論上可以與一個(gè)以上的DNA納米結(jié)構(gòu)進(jìn)行結(jié)合。結(jié)果與示意圖如下所示:
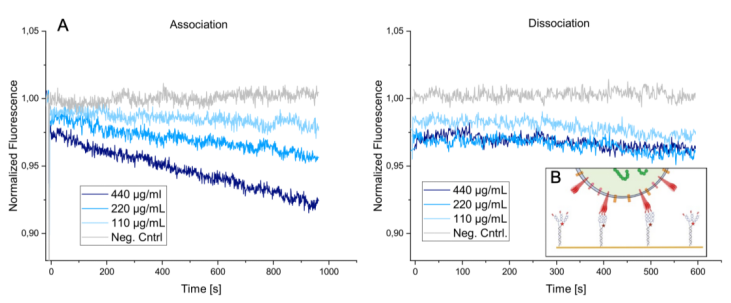
結(jié)果表明,在病毒顆粒結(jié)合期間,隨著病毒顆粒濃度的增加,可見熒光信號強(qiáng)度減弱加快,表明結(jié)合性能增強(qiáng);但病毒顆粒與配體的結(jié)合,呈現(xiàn)出線性結(jié)合,而非指數(shù)形式的結(jié)合曲線;在600s的解離時(shí)間內(nèi),未觀測到解離的發(fā)生,表明病毒顆粒與配體具有較強(qiáng)的結(jié)合性能。
本實(shí)驗(yàn)采用慢病毒包裝系統(tǒng),產(chǎn)生表達(dá)刺突蛋白的病毒顆粒。產(chǎn)生的病毒顆粒同樣使用化學(xué)誘導(dǎo)失活,并進(jìn)行純化和濃縮后用于動力學(xué)檢測。結(jié)果如下圖所示:
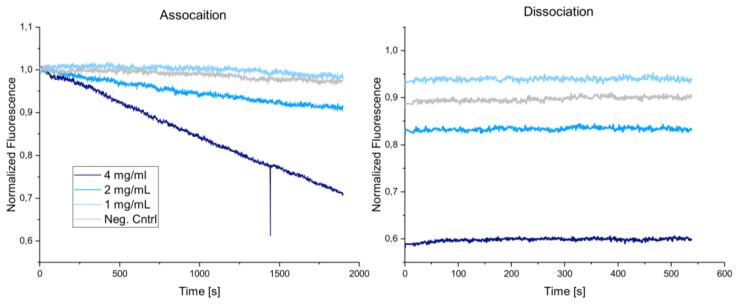
結(jié)果表明,隨著假病毒顆粒濃度的增加,顯示出與配體較強(qiáng)的結(jié)合性能,并且與上述病毒顆粒相同,結(jié)合曲線表現(xiàn)為線性變化, 600s的解離時(shí)間內(nèi),未觀測到解離的發(fā)生。在該實(shí)驗(yàn)中,病毒所需要的濃度要高于上述病毒顆粒,推測其原因是由于假病毒與天然病毒在樣本制備和樣本特性方面的各種差異所導(dǎo)致,比如刺突蛋白在兩種病毒顆粒上表達(dá)的密度等差異。
假病毒顆粒中的刺突蛋白可以經(jīng)由基因工程的方法進(jìn)行突變,構(gòu)建攜帶突變位點(diǎn)的假病毒顆粒。根據(jù)目前存在的SARS-CoV-2突變株,進(jìn)行假病毒的包裝。本實(shí)驗(yàn)中測試了三種不同的刺突蛋白突變體,命名為野生型(最初在中國武漢發(fā)現(xiàn)),B1.1.7或稱Alpha突變體(最初在英國發(fā)現(xiàn))和B1.351或稱Beta突變體(最初在南非發(fā)現(xiàn))。與野生型相比,兩種突變體均展現(xiàn)出了差異較大的結(jié)合性能。結(jié)果如下圖所示:
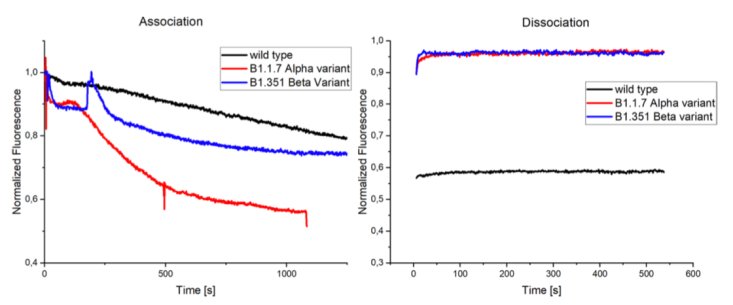
實(shí)驗(yàn)結(jié)果表明,三種病毒顆粒均展現(xiàn)出較強(qiáng)的結(jié)合性能,其中B1.1.7毒株展現(xiàn)出了最快最強(qiáng)的結(jié)合性能,其測試濃度也是最低的。與典型的野生型的線性結(jié)合相比,兩種突變毒株與配體肽的結(jié)合均出現(xiàn)指數(shù)的變化;在600s內(nèi)未觀測到解離的發(fā)生,表明其具有較強(qiáng)的結(jié)合能力。

heliX+ 分子互作分析系統(tǒng)

heliXcyto原生分子互作細(xì)胞分析系統(tǒng)
同騰睿杰(上海)生物科技有限公司作為Dynamic Biosensors中國總代理商,為您提供優(yōu)質(zhì)的售前售后服務(wù)。
聯(lián)系電話:021-50826962
聯(lián)系郵箱:sales@ttbiotech.com




